Osmometrie und Osmolalität
Osmolarität - Osmolalität
Mit diesen Begriffen werden im medizinisch-biologischen Bereich die Molkonzentrationen aller in einer Lösung osmotisch wirksamen Moleküle bezeichnet. Osmolarität ist die Molkonzentration bezogen auf das Volumen des Lösungsmittels. Osmolalität dagegen ist auf die Masse des Lösungsmittels bezogen. Mit Löser - Osmometern werden Osmolalitäten gemessen.Osmotischer Druck
In der Praxis ist Osmolalität ein Maß für die Gesamtzahl aller gelösten Teilchen in einer Lösung. Die Osmolalität x einer gegebenen wäßrigen Lösung definiert sich so: x = u x Nmol mit u = 1 bei einer undissozierten Lösung; ansonsten entspricht u der Gesamtanzahl der Ionen, die in einem Molekül der Lösung vorhanden sind oder sich gebildet haben. Nmol = Molzahl der undissoziierten Substanz.Die Einheit für die Osmolalität ist das Osmol (osm), im allgemeinen gebräuchlich ist das Milliosmol (mosm). Wenn nicht anders beschrieben, wird die Osmolalität durch die Gefrierpunktserniedrigung bestimmt. Zwischen dieser und der Osmolalität bestehen die nebenstehenden Beziehungen:
Meßprinzip
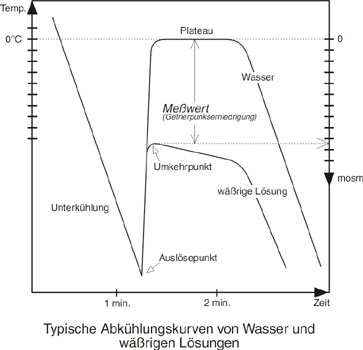
Es wird der Gefrierpunkt von wäßrigen Lösungen gemessen. Die Gefrierpunktserniedrigung im Vergleich zum reinen Wasser stellt ein direktes Maß für die osmotische Konzentration dar. Reines Wasser gefriert bei 0°C, eine wäßrige Lösung mit einer Osmolalität von 1 osmol / kg H2O bei -1,858°C. 1 Mol Substanz in einem kg H2O gelöst, ergibt nur dann eine Lösung mit der osmotischen Konzentration von 1 osmol / kg H2O, wenn es eine ideale Lösung ist und wenn die Substanz nicht dissoziiert.Wirkungsweise und Beschreibung
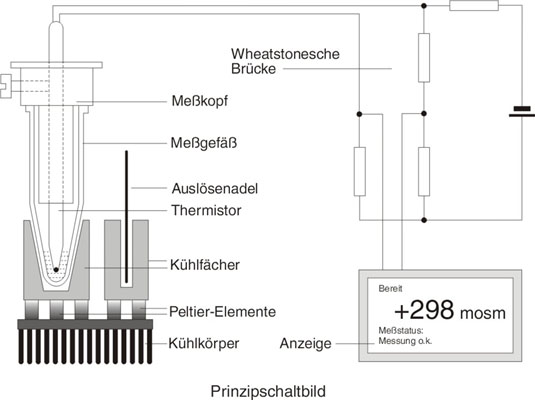
Bei Löser-Osmometern wird die Wärme über Kühlflächen an die Luft abgegeben, ein Wasseranschluß ist nicht erforderlich. Somit ist für den Betrieb lediglich eine Steckdose nötig. Die Temperatur der kalten Seite wird elektronisch konstant gehalten.
Während der Messung wird die Temperatur in der Probe von einem Thermistor (ein temperaturabhängiger Widerstand) gemessen. Dieser ist Bestandteil des Meßkopfes, an den das Meßgefäß gesteckt wird. Der Meßkopf ist an einer Führung befestigt, wo er vor unbeabsichtigter Beschädigung geschützt ist. Bei einer definierten Unterkühlung wird der Gefriervorgang ausgelöst, indem eine Nadel mit Eiskristallen in die Probe eingetaucht wird. Es stellt sich nun der Gefrierpunkt der Flüssigkeit ein. Die Methode des Auslösens ist entscheidend für die Reproduzierbarkeit der Messungen. Das kurzzeitige Eintauchen einer Nadel mit Eiskristallen ergibt genauere Meßergebnisse, als das Rühren mit einem ständig in die Probe eintauchenden Draht.
Wegen des linearen Zusammenhanges zwischen Osmolalität und Gefrierpunkt ist die Messung der Gefriertemperatur auch eine Messung der Osmolalität. Daher werden mosm / kg H2O direkt angezeigt.
Anwendungsgebiete für Osmometer